EBL-3183的工艺之路:从吲哚到临床前抑制剂
背景
金属β-内酰胺酶(MBLs)被视为决定碳青霉烯抗生素抗药性的主要因素。因此,寻找新的MBL抑制剂成为当前的紧迫任务。近期,Andrei Baran教授及其团队在Org. Process Res. Dev杂志上发表了一篇文章,详细介绍了MBL抑制剂“EBL-3183”的合成路径,以及如何通过优化合成工艺来提高产量和纯度,以满足临床前研究的需要。
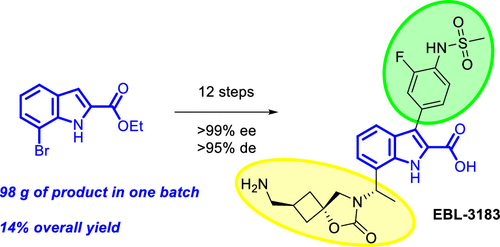
关于EBL-3183
EBL-3183作为一种新型的金属-β-内酰胺酶(MBLs)抑制剂,能有效干扰MBL的活性,提升抗生素的治疗效果。目前已进入临床前研究阶段。
EBL-3183是含有吲哚羧酸(InC)支架的新型化合物,具备优异的活性。尽管之前的候选化合物InC 1在体内外展现出卓越的抑制活性,但在安全性方面表现欠佳。因此,研究团队转向了类似物InC 2的研究,这类似物相较于InC 1在体内显示出更好的安全性,并且对碳青霉烯药物也表现出良好的增效作用。
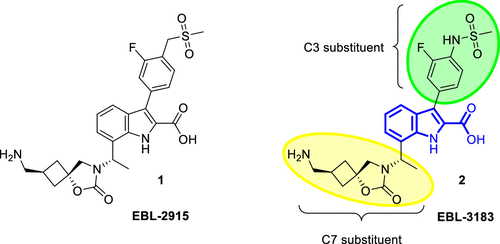
图1. 吲哚羧酸金属-β-内酰胺酶抑制剂 InC 1(EBL-2915)和 InC 2(EBL-3183)的结构。
合成策略
研究团队通过一项新的合成路线成功合成了候选化合物EBL-3183,并且已经在公斤级规模上实现了生产。这一合成工艺是以吲哚-2-羧酸酯为起始原料,通过埃尔曼辅助方法和钌催化的立体选择性还原引入手性。关键的螺环环丁烷基团则是通过精巧地组装环氧化物结构单元而来,这种结构单元能够以非对映纯形式获得,从而为合成过程提供了便利。
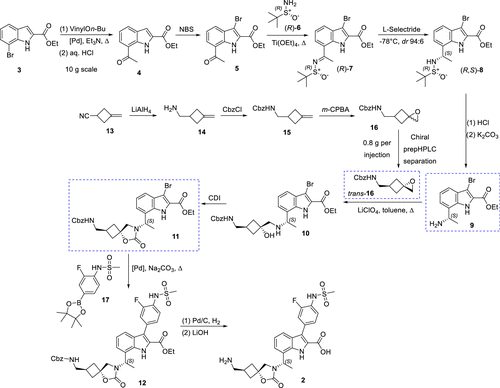
图 2. InC 2(EBL-3183)的药物化学路线
在合成过程中,(S)-7的制备是至关重要的一步,需要极具选择性的还原条件。通过选择性更好的还原剂和催化条件,能够有效地避免异构体的分离问题,同时提升产物的结晶性,进而简化了后续的纯化操作。此外,为了确保(S)-7的合成成功,必须严格把控钛试剂的质量,以防止杂质的生成。
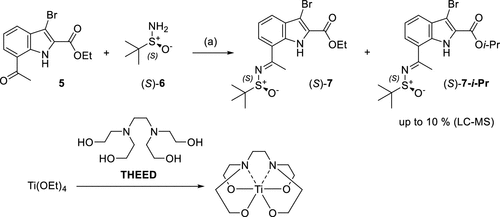
图3. Ti(OEt)4促进亚磺酰亚胺(S)-7a 的合成
实现目标化合物InC 2的大规模合成的关键之一是能够可扩展地实现立体选择性,以制备关键的螺环并联环丁烷-环氧化物trans-16。通过对易得的烯烃13进行环氧化反应,然后利用结晶和蒸馏分离目标异构体,成功地制备了环丁烷构建块trans-16'。这个过程采用了3个并行批次,平均产率为39%,得到了23克的trans-16'。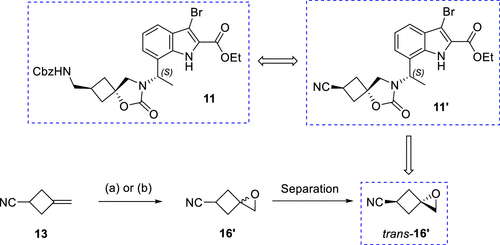
图 4.替代环丁烷结构分子砌块-氰基环氧化物反式-16'
制备中间体11'对于合成EBL-3183同样至关重要。通过环化反应可大量获得中间体11'(单批次可达160克)。该过程采用Suzuki-Miyaura交叉偶联反应完成。
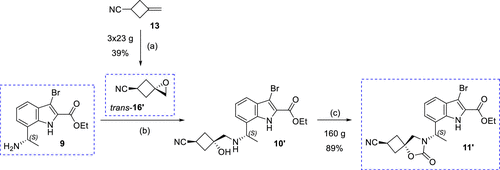
图 5.分子砌块反式-16′和中间体 11′的合成
另外,成功实施了腈还原步骤,确认了11'作为备用C3类似物合成的合适分子砌块。通过pH控制沉淀法进行可扩展的精制,使得目标化合物2(EBL-3183)的整体纯度提高到95.3-95.5%的充分水平,满足了临床前研究对高纯度的需求。
总结
总的来说,该合成路线是以吲哚3为起始物,经过六个关键步骤制备了手性结构分子砌块9,总产率达到了47%。通过结晶和蒸馏的手段成功分离出目标异构体,制备了高度立体选择性的环丁烷结构单元反式-16′。最终,通过五个步骤,总产率达到了29%,满足了足够规模和纯度的要求,获得了新型MBL抑制剂候选化合物(EBL-3183)。
参考文献
1.Andrei Baran,Jevgenijs Kuzmins. et al. Optimized Synthesis of Indole Carboxylate Metallo-β-Lactamase Inhibitor EBL-3183. Org. Process Res. Dev. 2023, 27, 4, 692–706. https://doi.org/10.1021/acs.oprd.3c00002
